

| top | 研究内容 | 研究業績 | 研究トピックス | メンバー | イベント | English |
|
主な研究課題 黄色ブドウ球菌はヒトをはじめとした哺乳類に常在する細菌であるが,疾病により免疫機能の低下した患者や乳幼児,老人に感染した場合は,各種の毒素,免疫撹乱物質などを産生し,敗血症や肺炎,黄色ブドウ球菌毒素ショック症候群などの重篤な疾患を引き起こす.これに加え,黄色ブドウ球菌は種々の抗生物質に対する耐性を容易に獲得するという劣悪な性質があり,すでに我々人類の保有するすべての抗生物質に対して薬剤耐性が獲得されてしまったことから,院内感染の原因菌として大きな社会問題となっている.このような背景から,黄色ブドウ球菌に対する創薬研究の社会的意義は深く,かつ急務であるが,有用な薬剤の獲得には至っていないのが現状である.
世の中には青い血の生き物が存在する.イカやタコ,貝などの軟体動物である.これらの生物はヘモシアニンという銅含有蛋白質を用いて酸素を運搬するため,その血は青いのである.ヘモシアニンは青いだけでなく,分子量が非常に大きいという特徴がある.イカのヘモシアニンは,約50kDaの機能ドメインが8個連結した約400kDaのポリペプチドが10個会合した巨大蛋白質会合体であり,その分子量は3.8MDaに及ぶ.興味深いことに,ヘモシアニンはその大きさを利用し,ハプテンのキャリア蛋白質やワクチン投与の際の免疫活性化剤として用いられている.このように医工学的に応用される一方で,その分子レベルでの解析は驚くほど進んでいない.これは,その大きさと解離しやすい性質から,これまでのヘモシアニンの構造学的研究は電子顕微鏡による低分解能の解析が中心であったためである.本研究では,X線結晶構造解析により,3.8MDaのスルメイカ由来ヘモシアニンの全体構造を3.0Aの分解能で決定した. 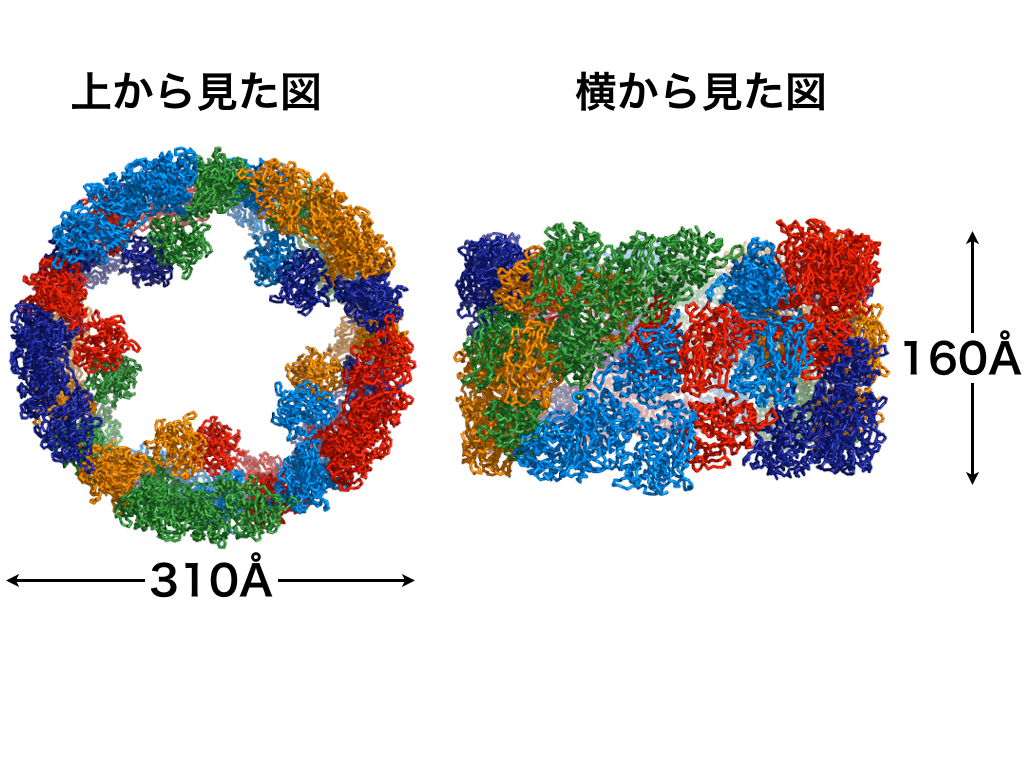 図1.スルメイカ由来ヘモシアニンの全体構造.3.8MDaにもおよぶ超巨大分子の原子座標を決定する事に成功した. 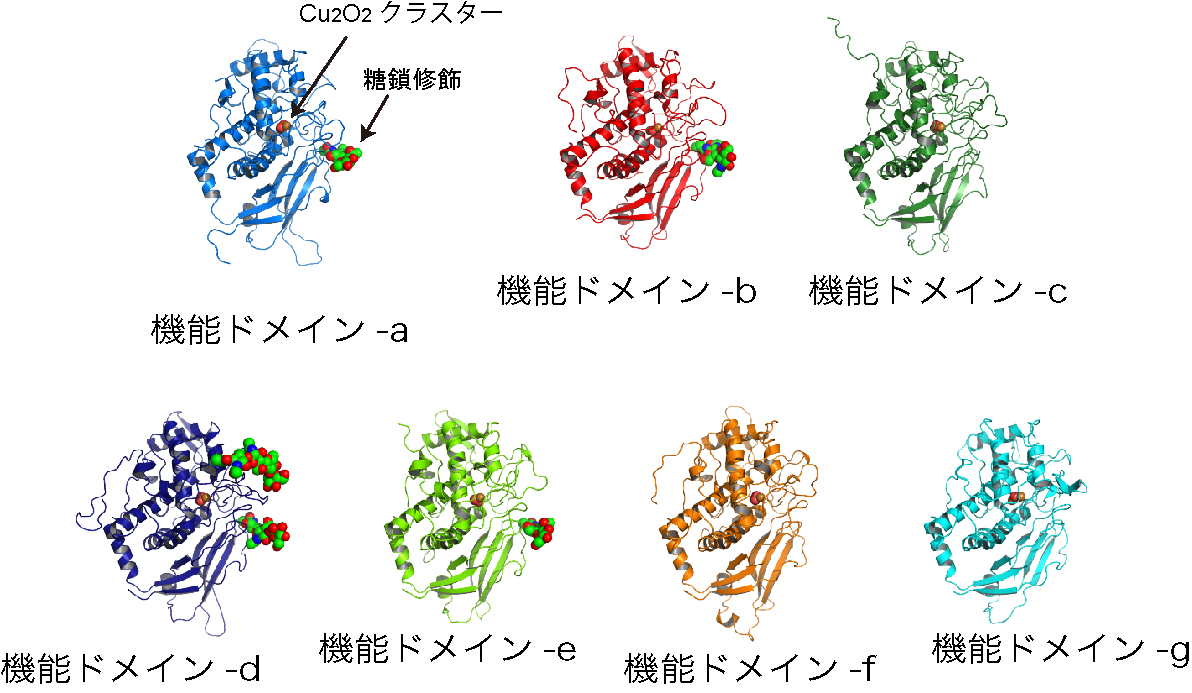 図2.サブユニットを構成する機能ドメインの構造
FtsZは真正細菌の細胞分裂に必須の蛋白質であり,新たな抗菌分子のターゲットとしても注目されている蛋白質である.細胞分裂過程において,FtsZは自己重合し直線状のフィラメントを形成する.さらに,このフィラメントの形状はFtsZの持つGTPaseによって湾曲化すると考えられている.我々は,FtsZ分子の立体構造変化がフィラメント内の分子間相互作用に影響を及ぼしフィラメントの湾曲化を引き起こすと予測し,FtsZやその変異体の立体構造解析を行った.構造解析の結果,我々は世界で初めてFtsZが2種類のコンフォメーションを持ち,各コンフォメーション間で構造遷移が生じる事を明らかにした (図1).また,FtsZと阻害化合物との複合体立体構造解析の結果,この阻害化合物がコンフォメーション変化に重要なヒンジ領域に結合することでFtsZの構造変化を抑制し,FtsZの機能と細胞分裂を阻害する阻害機構を提唱した (図2A).また,FtsZを阻害する新たな阻害活性分子の同定にも成功している (図2B). 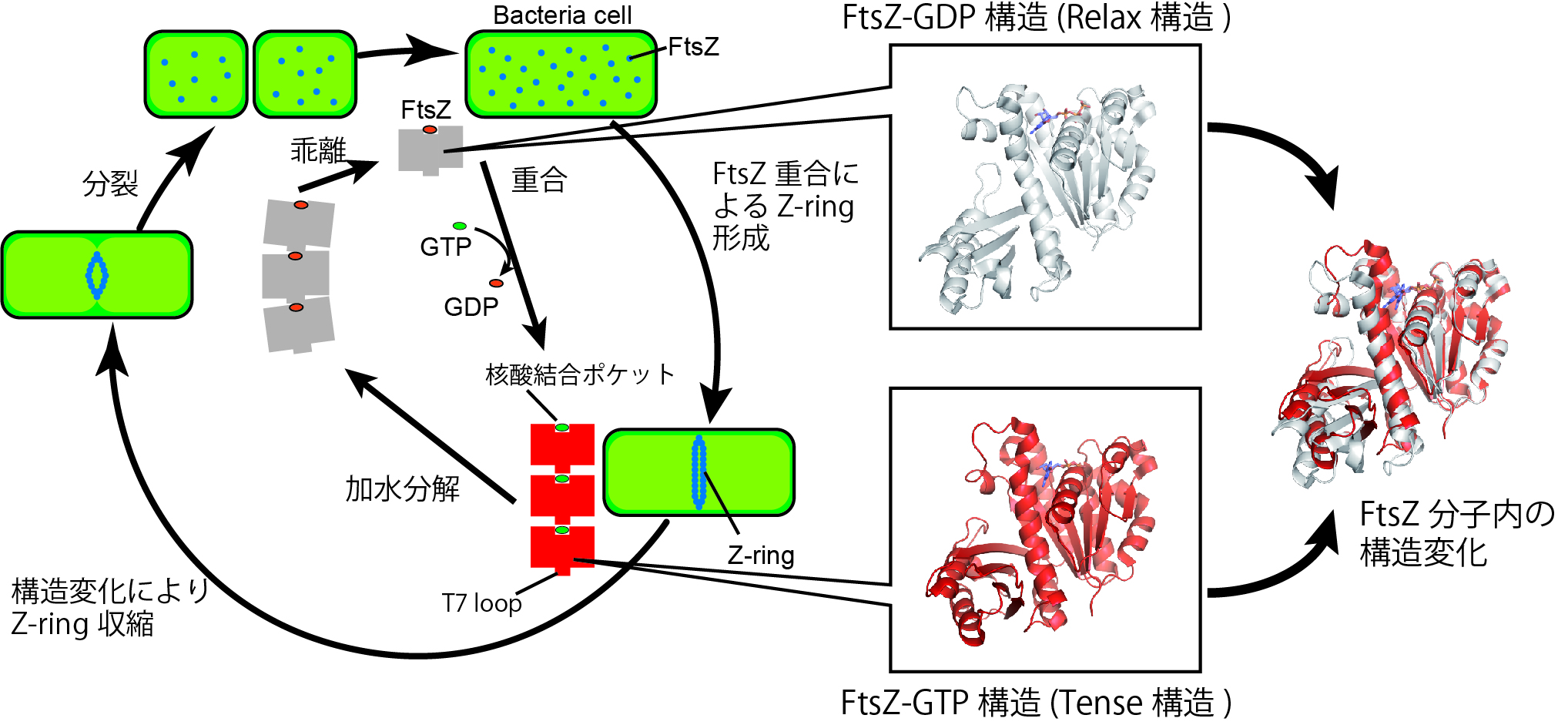 図1.細菌の細胞分裂におけるFtsZの構造変化. 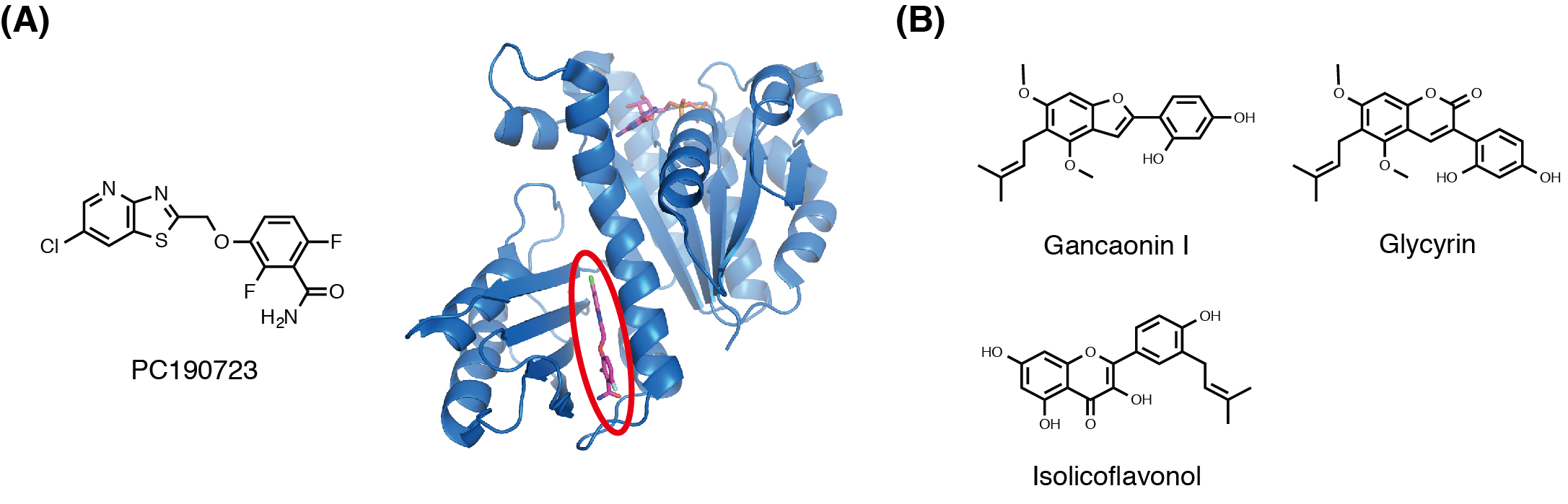 図2.FtsZ-化合物複合体結晶構造(A)と,カンゾウ由来のFtsZ阻害活性分子(B). 植物や微生物の二次代謝産物にはペニシリンを始めとした非常に多くの抗菌活性低分子化合物が見出されている.これまでに,ペプチド系抗生物質や抗菌活性を持つアルキルキノロン等の生合成酵素の立体構造解析による触媒反応機構を明らかにしている.さらに,立体構造情報を活用し,触媒活性部位を改変して非天然基質を受入れ新規抗菌活性分子を創生可能な人工酵素の開発も進めている. |